- · 中国医院院长版面费是多[07/01]
- · 《中国医院院长》投稿方[07/01]
- · 《中国医院院长》期刊栏[07/01]
首都医科大学宣武医院副院长卢洁教授:AI在脑脱
作者:网站采编关键词:
摘要:机器学习模型由高维的组学特征组成,所以其解释性相对来说比较差,不容易理解。SHAP是目前比较流行的一种模型解释方法,通过计算在合作中每个个体的贡献来确定个体的重要程度。

机器学习模型由高维的组学特征组成,所以其解释性相对来说比较差,不容易理解。SHAP是目前比较流行的一种模型解释方法,通过计算在合作中每个个体的贡献来确定个体的重要程度。本模型具有可解释性,对于case A,随机森林模型判断有89%可能性是MS,其中最主要的贡献来自H-MPR-Log_95这个特征,我们可以把每一个特征的贡献值计算出来。
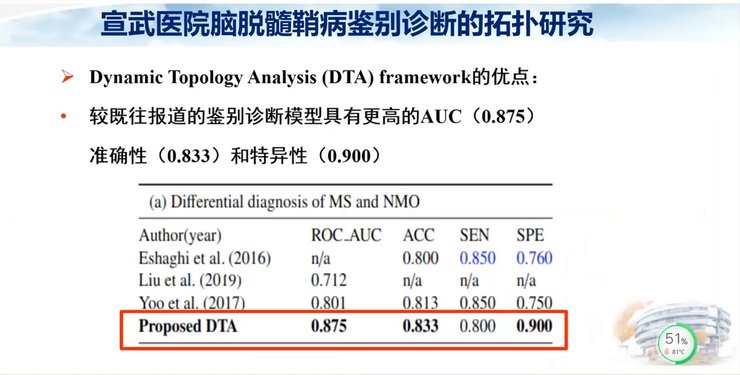
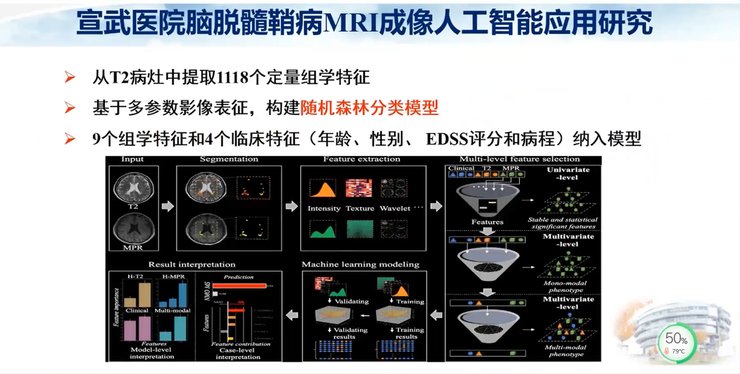
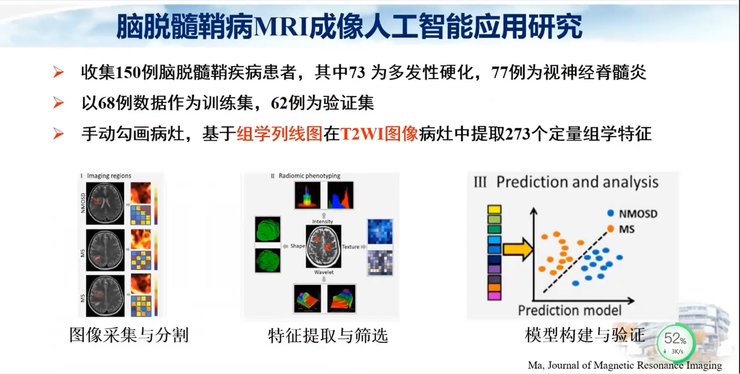
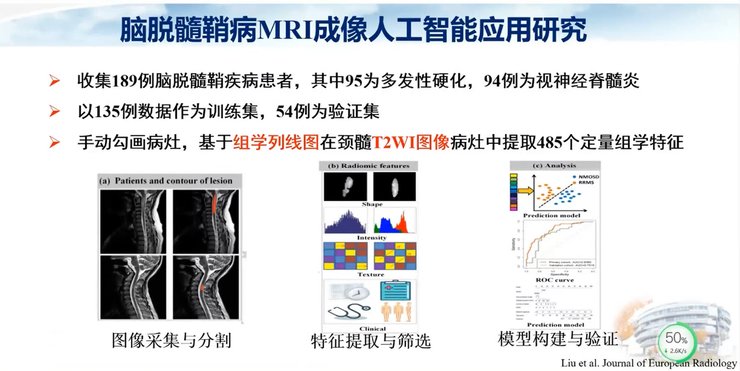
在脑脱髓鞘病MRI成像人工智能应用研究中,我们收集到150例患者,其中73例为多发性硬化,77例为视神经脊髓炎。我们以68例患者作为训练集,62例作为验证集,手动勾画病灶,基于组学列线图在T2WI图像的病灶中提取了273个定量组学特征。
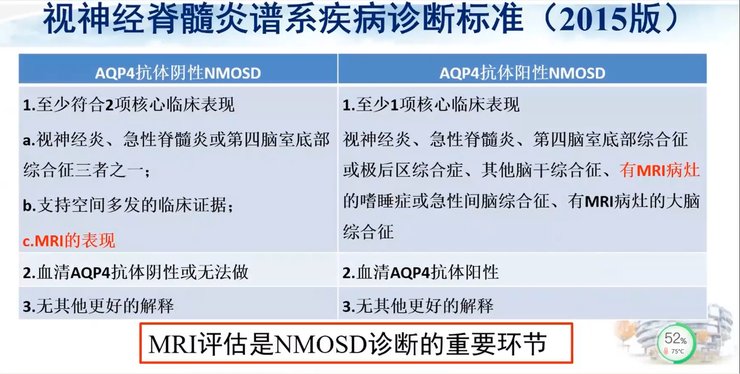
视神经脊髓炎的诊断标准多年来经历了数次演变,1894年首次提出NMO的概念;1999年出现第一个NMO诊断标准;2004年AQP4-lgG发现后,NMO被认为是不同于MS的独立疾病;2007年提出了NMOSD(视神经脊髓炎谱系疾病)的新概念;2015年出现了最新的NMOSD诊断共识。
首都医科大学宣武医院副院长卢洁教授作为本次大会的嘉宾,以《脑脱髓鞘病MRI成像的人工智能应用研究》为题发表了演讲。
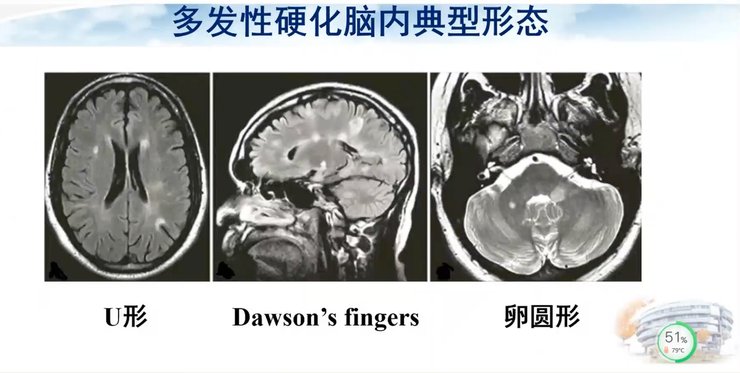
临床中应用的常规磁共振成像可以为多发性硬化提供多维度的信息,包括病灶数量、位置、体积,以及强化的特点和病灶进程。而且,常规磁共振诊断多发性硬化的灵敏度较高,可达到约95%。
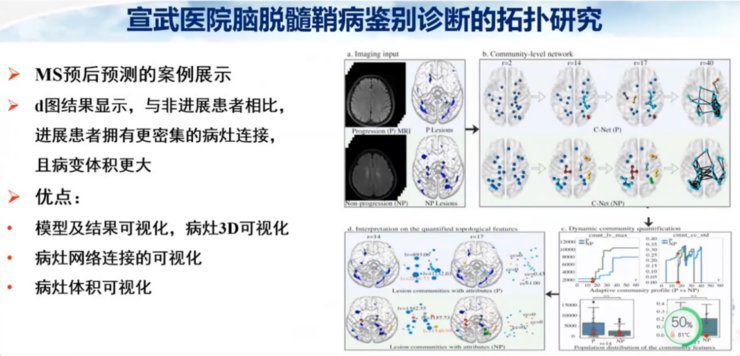
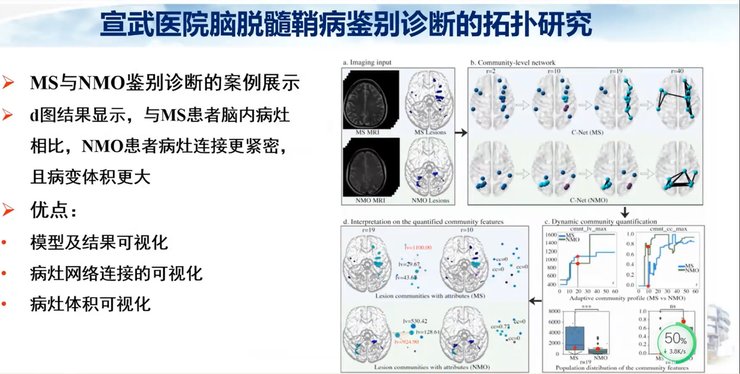
通过磁共振纵向随访研究发现,慢性病灶具有融合的趋势,而且临床的残疾程度会逐渐增加。所以我们提出假设随着疾病的进展,病灶的拓扑性质发生改变;反之,病灶拓扑结构变化也具有潜在的预测作用。
MS与NMOSD的鉴别诊断十分具有挑战性,根据既往文献的报道,大约30%的MS患者在疾病早期会被误诊为NMOSD。这两种疾病的临床症候比较相似,实验室检查结果也有部分重叠,因此确诊周期较长,大约12%的患者需要至少6年时间才能确诊。对基层医院的医生与低年资医生来说,这两种疾病的诊断更具有挑战性。
我们来看一下组学列线图,它是建立在多因素回归分析的基础上,将多个预测指标进行整合,然后采用带有刻度的线段,按照一定比例绘制在同一平面上,从而用来表达预测模型中各个变量之间的相互关系。


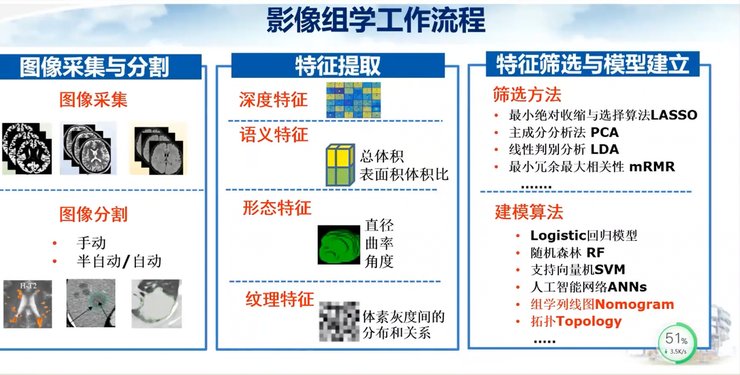
这是具体的影像组学工作流程图,从图像采集与分割,到深度特征、语义特征、形态特征及纹理特征的提取,再到进行特征筛选与模型构建。特征筛选和建模均有很多方法可供选择。
这部分研究共收集了90例进展的MS和54例非进展MS,如果残疾量表增高1.5分以上就定义为进展,小于1.5分定义为非进展,用T2WI数据进行训练。通过对病灶进行勾画提取多发病灶的空间模式。
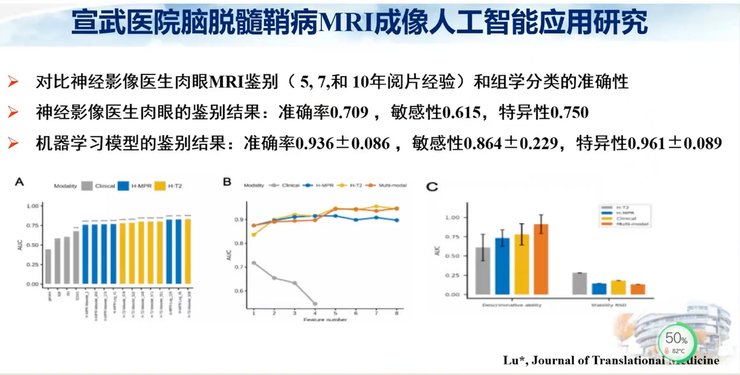
人工智能辅助鉴别诊断同样具有挑战性,主要在于基于单一的临床数据库、基于单一序列、基于单一磁共振仪,组学列线图仍缺乏可解释性,且缺乏人工智能模型和临床医生判读的对比。
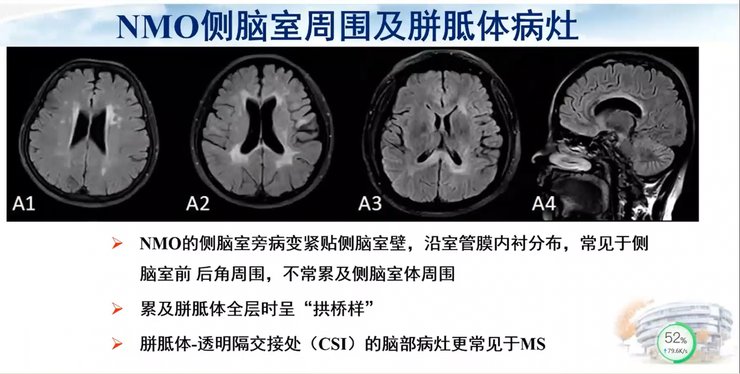
我们也可以将拓扑在脑脱髓鞘疾病的诊断中进行应用。由于MS和NMO两种疾病的发病机制不同,其脑内病灶的空间分布不同,形态、大小也不相同,所以这两种疾病的脑内病灶的拓扑性质并不相同,我们希望能够找到潜在的鉴别诊断突破点。

视神经脊髓炎也是中枢神经系统常见的炎性脱髓鞘疾病,发病率仅次于多发性硬化,在亚洲更加多见,尤其以女性多发,男女比例大约是1:4。该病主要累及视神经、脊髓、脑,血清特异性自身抗体为AQP4抗体阳性。85%-90%患者会复发,预后比多发性硬化更差。
多发性硬化、视神经脊髓炎是常见的脑脱髓鞘病,但是二者的鉴别诊断困难;而人工智能可以帮助挖掘影像图像中肉眼无法识别的高维定量特征;基于拓扑的人工智能模型在预测脑脱髓鞘病预后中具有重要的价值,未来我们也希望在这方面进行更深入的探索。
文章来源:《中国医院院长》 网址: http://www.zgyyyc.cn/zonghexinwen/2022/1026/361.html